
Она смешивается с водой в любых соотношениях со значительным выделением теплоты (образуются гидраты). В серной кислоте растворяется оксид серы. Такой раствор, состав которого характеризуется содержанием свободного SО3(100%-я H2SO4), называется олеумом. ГОСТ 2184-77 является межгосударственным стандартом кислоты серной технической. Настоящий стандарт распространяется на техническую серную кислоту следующих видов: контактную (улучшенную и техническую); олеум (улучшенный и технический); башенную и регенерированную. | Наименование показателя | Норма | | Контактная | Олеум | Башенная | Регенериро-ванная | | Улучшенная | Техническая | Улучшенный | Технический | | 1-й сорт | 2-й сорт | | 1. Исключен (Изм. № 3). | | | 2. Массовая доля моногидрата (H2SO4), % | 92,5-94,0 | Не менее 92,5 | Не нормируется | Не менее 75 | Не менее 91 | | 3. Массовая доля свободного серного ангидрида (SO3), %, не менее | - | - | - | 24 | 19 | - | - | | 4. Массовая доля железа (Fe), %, не более | 0,006 | 0,02 | 0,1 | 0,006 | Не нормируется | 0,05 | 0,2 | | 5. Массовая доля остатка после прокаливания, %, не более | 0,02 | 0,05 | Не норми-руется | 0,02 | То же | 0,3 | 0,4 | | 6. Массовая доля окислов азота (N2O3), %, не более | 0,00005 | Не нормируется | 0,0002 | Не нормируется | 0,05 | 0,01 | | 7. Массовая доля нитро-соединений, %, не более | Не нормируется | 0,2 | | 8. Массовая доля мышьяка (As), %, не более | 0,00008 | Не нормируется | 0,00008 | Не нормируется | | 9. Массовая доля хлористых соединений (Cl), %, не более | 0,0001 | Не нормируется | | 10. Массовая доля свинца (Pb), %, не более | 0,001 | Не нормируется | 0,0001 | Не нормируется | | 11. Прозрачность | Прозрачная без разбавления | Не нормируется | | 12. Цвет, см3 раствора сравнения, не более | 1 | 6 | Не нормируется | Источник: ГОСТ 2184-77 Сырье для производства Сырьем в производстве серной кислоты могут быть элементарная сера и различные серосодержащие соединения, из которых может быть получена сера или непосредственно оксид серы (IV). Природные залежи самородной серы невелики, хотя кларк ее равен 0,1 %. Чаще всего сера находится в природе в форме сульфидов металлов и сульфатов метало, а также входит в состав нефти, каменного угля, природного и попутного газов. Значительные количества серы содержатся в виде оксида серы в топочных газах и газах цветной металлургии и в виде сероводорода, выделяющегося при очистке горючих газов. Таким образом, сырьевые источники производства серной кислоты достаточно многообразны, хотя до сих пор в качестве сырья используют преимущественно элементарную серу и железный колчедан. Ограниченное использование таких видов сырья, как топочные газы тепловых электростанций и газы медеплавильного производства, объясняется низкой концентрацией в них оксида серы (IV). При этом доля колчедана в балансе сырья уменьшается, а доля серы возрастает. В общей схеме сернокислотного производства существенное значение имеют две первые стадии – подготовка сырья и его сжигание или обжиг. Их содержание и аппаратурное оформление существенно зависят от природы сырья, которая в значительной степени, определяет сложность технологического производства серной кислоты. Технология производства Производство серной кислоты из серосодержащего сырья включает несколько химических процессов, в которых происходит изменение степени окисления сырья и промежуточных продуктов. Это может быть представлено в виде следующей схемы: 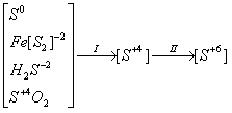 где I – стадия получения печного газа (оксида серы (IV)), II – стадия каталитического окисления оксида серы (IV) до оксида серы (VI) и абсорбции его (переработка в серную кислоту). В реальном производстве к этим химическим процессам добавляются процессы подготовки сырья, очистки печного газа и другие механические и физико-химические операции. В общем случае производство серной кислоты может быть выражено в следующем виде: Сырье  подготовка сырья подготовка сырья  сжигание (обжиг) сырья сжигание (обжиг) сырья   очистка печного газа очистка печного газа  контактирование контактирование  абсорбция абсорбция
контактированного газа  СЕРНАЯ КИСЛОТА СЕРНАЯ КИСЛОТА Конкретная технологическая схема производства зависит от вида сырья, особенностей каталитического окисления оксида серы (IV), наличия или отсутствия стадии абсорбции оксида серы (VI). В зависимости от того, как осуществляется процесс окисления SО2 в SО3, различают два основных метода получения серной кислоты. В контактном методе получения серной кислоты процесс окисления SО2 в SО3 проводят на твердых катализаторах. Триоксид серы переводят в серную кислоту на последней стадии процесса – абсорбции триоксида серы, которую упрощенно можно представить уравнением реакции: SО3 + Н2О 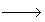 Н2SО4 Н2SО4 При проведении процесса по нитрозному (башенному) методу в качестве переносчика кислорода используют оксиды азота. Окисление диоксида серы осуществляется в жидкой фазе и конечным продуктом является серная кислота: SО3 + N2О3 + Н2О 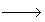 Н2SО4 + 2NО Н2SО4 + 2NО В настоящее время в промышленности в основном применяют контактный метод получения серной кислоты, позволяющий использовать аппараты с большей интенсивностью. |
