Белковая инженерия Казеин, продукты переработки животного и рыбного сырья, кровь и соя, все эти вещества используются для производства клеев, в составе которых длинные белковые цепи выполняют функции полимеров. Особенно хорошо связи в животных клеях образуются в результате охлаждения и получения геля, а также потери воды, при этом образуется интересное сочетание горячего расплава и связывающего вещества на водяной основе. При воздействии экстремальных температур, а также кислотных или щелочных условий природные формы денатурированных казеинов отделяются от тех трехмерных структур, в состав которых они ранее входили, и становятся выделенными полимерными белками. После этого их можно использовать при разработке рецептур связывающих веществ. Молекулярную массу белка можно подобрать за счет специальных реакций гидролиза, затем его можно высушивать или компаундировать в зависимости от намеченного применения. Коллаген является основным связывающим белком в организмах животных, его также можно легко получать из рыб, что является общей отправной точкой для белковых связывающих веществ. Для получения более высокой прочности коллагеновых связывающих веществ, могут быть образованы внутримолекулярные поперечные связи за счет кислородного дезаминирования особых лизиновых и гидроксилизиновых мономеров в белковых полимерных цепях для формирования альдегидов.4 В присутствии медного катализатора, эта реакция происходит за счет конденсации альдоля, которая преобразует аминогруппы лизинов в альдегиды. Эти альдегиды затем вступают в реакцию с не модифицированным лизином и гидроксилизином для формирования иминов, что также известно как шиффово основание или же альдаминовое сшивание. 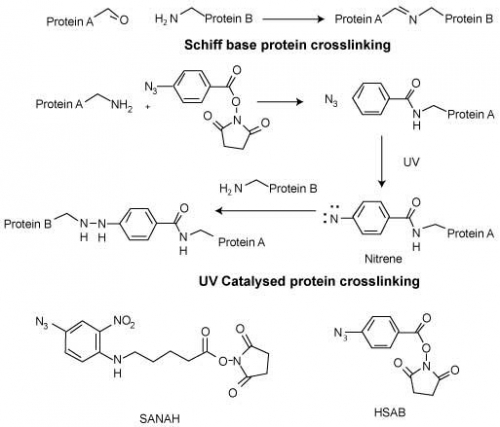
Рис. 2: Повышение управляемости сшиванием в белковых связывающих веществах Недавно были разработаны методы ультрафиолетового управления сшиванием с использованием гетеробифункциональных реактивов, таких как 4-азидобензойная кислота N-гидроксисукцинимидный эфир (HSAB) и 6-(4-азидо-2-нитрофенил-амино) капроновая кислота N- гидроксисукцинимидный эфир (SANAH). Сначала только один конец бифункционального реактива образует аминовые связи с основным белковым полимером, другой же конец остается несвязанным до фотокатализа с помощью коротковолновых ультрафиолетовых световых волн. Этот конец затем превращается в высоко реактивный нитрен или карбен, который быстро начинает образовывать дополнительные поперечные связи. Ультрафиолетовый катализ обеспечивает высокую степень управления отверждением связывающего вещества, и его более прочной адгезией, этот метод хорошо подходит для различных биологических применений.
| 