
При небольшом количестве электролитов их названия могут основываться на случайных определениях, зависящих исключительно от предпочтений разработчика: номерах, специфических свойствах получаемых покрытий, особенностях проведения процесса или на фамилии разработчика. С учётом того, что к настоящему времени разработано сотни электролитов, имеет особое значение их классификация (в этих условиях немыслимо представить себе произвольную классификацию, основанную, на пример, только лишь на номере электролита: электролит № 1, электролит № 2 и т.д. - не только непонятно о чём идёт речь, но и непонятно в области какой технологии мы находимся). Для взаимопонимания специалистов и осознания разработчиками технологий своего места в гальванотехнике традиционно сложилась (прижилась) классификация простого типа, основанная на выработке названия электролита по наименованию основных компонентов, входящих в его состав. Под основными компонентами понимают в первую очередь вещества, играющие главную роль в протекании процесса. Например, для электролитов нанесения катодных покрытий такими веществами являются кислотные остатки, лиганды и в некоторых случаях органические добавки, которые определяют стандартный потенциал, поляризацию и поляризуемость (рис. 1 [1]). 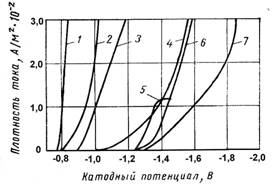
Рис. 1. Относительное расположение поляризационных кривых при электроосаждении цинка из различных электролитов без перемешивания: 1 - сульфатный; 2 - сульфатный с декстрином; 3 - хлораммиакатный (аммиакатнохлоридный); 4 - пирофосфатный; 5 - цинкатный; 6 - цинкатный с ПЭИ; 7 - цианидный
При анодировании алюминия названия электролитов определяются названием компонента, который определяет скорость роста барьерного слоя оксидов алюминия и скорость его растворения: сульфатные, оксалатные (щавелевокислые), хромовокислые, сульфосалициловые и т.д. электролиты. При химическом травлении металлов названия электролитов определяется названием основных кислот или щелочей, способствующих растворению металла. И так далее.
Таким образом, все электролиты для нанесения конкретного вида покрытия (цинкования, кадмирования, меднения, оловянирования, никелирования, хромирования, латунирования, палладирования и т.п.) делятся на следующие группы: 1 (простые, так называемые "кислые", не в смысле величины рН, а вследствие того, что эти электролиты содержат кислоту в виде свободного кислотного остатка, который не является лигандом для осаждаемого металла) - сульфатные, хлоридные, фторидные, нитратные, хлорсульфоновые, фторборатные, кремнефторидные, щелочные (не в смысле величины рН, а вследствие наличия в составе электролита свободной щелочи, не образующей комплексы с ионами осаждаемого металла), фосфатные и т.п., в которых металл, формирующий покрытие, находится в виде простых гидратированных соединений; 2 (комплексные) - аммиакатные, трилонатные, оксалатные, цитратные, ацетатные, уротропиновые, салицилатные, гликоколевые, щелочные (не в смысле величины рН, а вследствие наличия в составе электролита щелочи, образующей гидроксокомплексы с ионами осаждаемого металла - цинкатные в случае цинкования, станнатные и станнитные в случае оловянирования и т.п.), пирофосфатные, цианидные, этилендиаминовые и т.д., в которых металл, формирующий покрытие, находится в виде комплексных соединений; 3 (смешанные) - аммиакатнохлоридные, сульфатноуротропиновые, оксалатносульфатные, аммиакатногликоколевые и т.п., в которых металл, формирующий покрытие, находится в виде сложных комплексных соединений. Существование третьей группы обсуждаемо.
|
