Крошечные организмы обладают массой преимуществ в качестве синтезаторов хоть горючего, хоть ещё каких-нибудь полезных смесей и соединений. Микробы очень быстро размножаются и неприхотливы в условиях. Беда одна: пока нам почти неизвестны бактерии, которые "гнали" бы высшей пробы "бензин" или "дизель". Хотя есть близкие примеры. Нашлась же в природе бактерия, которая генерирует гидразин из сточных вод.
А если подкорректировать геном какой-нибудь бактерии (хоть самой популярной у биологов – кишечной палочки), да так, чтобы она выдавала требуемые вещества как продукт своего метаболизма? К примеру, "научили" же генетики кишечную палочку синтезировать пластмассу. Этим и занята LS9, смешавшая в своих исследованиях давно известную биоинженерию и сравнительно молодую науку — синтетическую биологию. Только одно мешает учёным хоть завтра перевести весь топливный сектор на биотехнологические рельсы – никто в точности не знает, как именно нужно менять геном бактерий, чтобы выход полезного вещества был максимальным. Наука тут отстаёт от практики. О практике – чуть позже, а пока поясним. Конечно, у учёных есть различные варианты коррекции генома, которые сдвигают биохимические реакции внутри бактерии в нужную сторону. Но стоит только применить одну из них, как оказываются затронутыми другие цепочки превращений, возникают вредные побочные эффекты. Добавление чужеродных генов или "заглушение" старых влияет не только на "нужные" процессы в клетке, но и на цепь смежных. И таких взаимоувязанных реакций в организме – миллионы. Начинают исследователи корректировать одни свои ошибки – вновь затрагиваются полезные перемены. Канитель, одним словом. 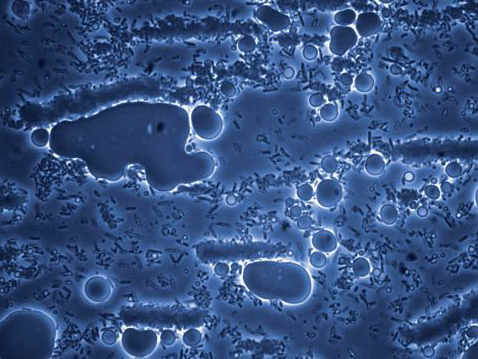
Трудолюбивые кишечные палочки (E. coli), плавающие в чашке Петри, обращают сахар в капельки углеводородов. Такую картину сейчас наблюдают в окуляры исследователи сразу из нескольких институтов и биотехнологических компаний. LS9 – только одна из них, но у неё есть преимущество: в то время как остальные проводят опыты с генетическими модификациями бактерий при помощи "кремниевых ружей", LS9 взяла на вооружение "пулемёт" (фото Amyris Biotechnologies). Фактически биологам приходится действовать методом проб, проверяя получающиеся организмы на полезный выход целевого соединения (или нескольких веществ сразу) и на жизнеспособность. Добавляют в геном один ген, дают бактериям размножиться – смотрят на результат. Слишком долго. Таким путём желаемый штамм можно искать месяцами, а то и годами. Разработка Чёрча сокращает этот срок до дней. Для этого Джордж и его товарищи применяют оригинальную технологию MAGE (multiplex-automated genomic engineering), то есть "умножено-автоматизированную геномную инженерию". В её основе – новое устройство, которое вполне можно было бы назвать "Машиной эволюции" (она и показана на фото под заголовком). Этот аппарат позволяет проводить с бактериями одновременно по 50 искусственных генетических изменений, то есть апробировать на микробах по полсотни экспериментальных генетических кодов за раз. Сначала учёные готовят 50 коротких цепочек ДНК, представляющих собой один и тот же участок генома бактерии, но с 50 разными вариациями, способными повлиять на синтез определённого фермента или белка. Эти 50 цепочек помещают вместе с бактериями в специальную машину, в которой смесь подвергается определённым изменениям температуры и в которой запускается цепочка реакций, приводящих к встраиванию привнесённого участка кода в геном бактерий.
| 