Факт образования фенола при комнатной температуре в рассматриваемой реакции наводит на мысль о вероятном сходстве α-кислорода с активным кислородом монооксигеназ, для которых гидроксилирование ароматических соединений является типичной реакцией [17, 18, 91]. Напомним, что монооксигеназами называют ферменты, способные при комнатной температуре селективно вести окислительные реакции, в ходе которых один атом кислорода, переведенный в активное состояние, присоединяется к неактивированной молекуле углеводорода-субстрата, давая ОН-содержащее соединение, а второй - расходуется на образование воды. Активация кислорода является наиболее трудной проблемой биомиметической химии, особенно в случае моделирования так называемых метанмонооксигеназ. Биядерные Fe-содержащие центры метанмонооксигеназ способны генерировать кислородные частицы, которые по активности значительно превосходят кислород других монооксигеназ. Вследствие этого, помимо способности гидроксилировать ароматические и другие соединения, метанмонооксигеназы обладают уникальной возможностью гидроксилировать даже метан наиболее инертную органическую молекулу.Изучение реакции α-кислорода с метаном [85, 92] с использованием той же трехстадийной схемы титрования, что и в вышеприведенном случае с бензолом («посадка» Oα, его взаимодействие с метаном при комнатной температуре и экстракция продукта) показало, что реакция протекает очень быстро, с образованием только метанола, количество которого соответствует количеству прореагировавшего метана. Аналогичные результаты были получены для реакций с этаном, пропаном и рядом других углеводородов: окисление α-кислородом при комнатной температуре приводит к образованию тех же продуктов, что и при окислении с помощью монооксигеназ. Для установления более глубокой аналогии α-кислородного окисления с биологическим окислением важно сравнить не только продукты, но и механизм, по которому они образуются в обоих случаях. Удобным инструментом для этой цели является измерение кинетического изотопного эффекта (КИЭФ). Известно, что биологическое окисление метана протекает с большим изотопным эффектом (от 5 до 12), тогда как в случае окисления бензола кинетический эффект не наблюдается [93]. Для сопоставления механизмов обсуждаемых процессов в работе [94] было проведено измерение КИЭФ для реакций окисления метана и бензола α-кислородом. Молекулы метана CH2D2, которые использовались в работе [94], могут реагировать либо по C-H, либо по C-D связи, давая две изотопные разновидности мета Экстрагированный с поверхности катализатора метанол был проанализирован методом ЯМР и на основании ЯМР-спектров рассчитаны величины изотопного эффекта. Оказалось, что в зависимости от температуры КИЭФ меняется от 5,5 при -50 оС до 1,9 при +100 оС. Высокие значения КИЭФ убедительно указывают на тот же механизм реакции, что и при окислении с помощью метанмонооксигеназ. В обоих случаях лимитирующая стадия реакции включает разрыв связи С-Н. 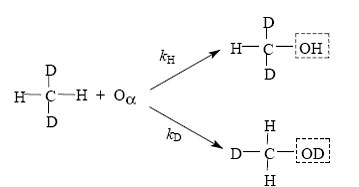
При взаимодействии α-кислорода с бензолом также образуются две изотопные разновидности фенола, содержащие ОН- и OD-группы. Результаты измерения КИЭФ и здесь показали сходство с биологическим процессом: как и в случае действия монооксигеназ, окисление бензола α-кислородом протекает без изотопного эффекта. Это значит, что лимитирующая стадия реакции не включает разрыв C—H связи и, вероятно, протекает через промежуточное образование ареноксида [94]: 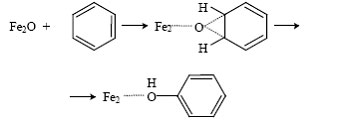
Таким образом, α-кислород во многих отношениях аналогичен активному кислороду метанмонооксигеназ: он координирован на комплексах Fe, обладает высокой реакционной способностью и направляет окисление по механизму того же типа.
|
