В молекуле жирной кислоты есть цепочка из метиленовых групп СН2, которая на одном конце заканчивается метильной группой –СН3, а на другом – карбоксильной группой –СООН. В кристалле эти цепи образуют параллельные цепочки, при этом две соседние карбоксильные группы притягиваются друг к другу за счет водородных связей гораздо сильнее, чем две метильные или метиленовые группы соседних молекул. В результате межмолекулярных взаимодействий молекулы карбоновых кислот образуют в кристаллах парные слои, в которых карбоксильные группы направлены навстречу друг другу. Углеводородные же цепи располагаются наклонно относительно плоскости, разделяющей два соседних слоя, как показано на рисунке. При этом угол наклона цепей зависит от четности молекулы, т.е. от того, «смотрят» ли концевые группы СН3 и СООН в одну или в разные стороны относительно оси молекулы (от этого зависит «удобство» упаковки цепей). Разный угол наклона цепей приводит к разной энергии взаимодействия между слоями четных и нечетных кислот. Объясняется это тем, что в зависимости от этого угла между карбоксильными группами возможно образование одной или двух водородных связей, как это показано на рисунке. Лишняя водородная связь, да еще умноженная на огромное число молекул в слое, существенно упрочняет кристаллическую решетку. 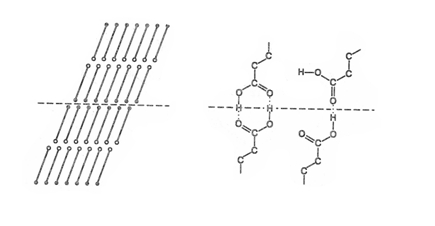
Рис. 2. СХЕМА ПОСТРОЕНИЯ КРИСТАЛЛА КАРБОНОВОЙ КИСЛОТЫ (слева). Черные кружки – карбоксильные группы, белые – метильные; пунктиром обозначена плоскость, разделяющая парные слои. Справа показаны два типа возможных взаимодействий между карбоксильными группами двух цепочек: с двумя водородными связями и с одной связью Когда цепи становятся достаточно длинными, взаимное притяжение двух соседних цепочек друг к другу становится преобладающим (по сравнению с притяжением двух соседних карбоксильных групп); в результате прочность кристаллической решетки практически перестает зависеть от «четности» молекулы и определяется только ее длиной, что и подтверждается экспериментально. «Приключения» маргариновой кислоты. В приведенной таблице есть единственное исключение из общего «четно-нечетного» правила для жирных кислот с n > 10. Это исключение – маргариновая кислота (С17). Название это происходит от греческого слова margaron – жемчуг и придумал его в начале 19 в. французский химик Мишель Эжен Шеврёль. Сейчас число известных природных жирных кислот исчисляется многими сотнями, правда, большинство их (в том числе и нечетных) содержится лишь вочень малых количествах. Очевидно, что биосинтез жирных кислот иногда может начинаться не с ацетил-КоА, а с пропионил-КоА – как у подопытных мышей. Нужны ли такие кислоты организму, или это вредный (а может быть, нейтральный) побочный продукт его жизнедеятельности? Однозначный ответ на этот вопрос пока еще не найден. Ненасыщенные монокарбоновые кислоты. Простейшая непредельная кислота, акриловая СН2=СНСООН, имеет острый запах (на латыни acris – острый, едкий). Акрилаты (эфиры акриловой кислоты) используются для получения органического стекла, а ее нитрил (акрилонитрил) – для изготовления синтетических волокон. В природных источниках в виде сложных эфиров содержится множество непредельных кислот. Высшие непредельные кислоты, как правило, содержат четное число атомов углерода и названы по природным источникам. Называя вновь выделенные кислоты, химики нередко дают волю фантазии. Так, название ближайшего гомолога акриловой кислоты, кротоновой СН3–СН=СН–СООН, происходит вовсе не от крота, а от растения Croton tiglium, из масла которого она была выделена. Очень важен синтетический изомер кротоновой кислоты – метакриловая кислота СН2=С(СН3)–СООН, из эфира которой (метилметакрилата), как и из метилакрилата, делают прозрачную пластмассу – оргстекло. Когда были открыты две изомерные кислоты, имеющие строение СН3–СН=С(СН3)–СООН, их назвали ангеликовой и тиглиновой. Ангеликовая кислота была выделена из ангеликового масла, полученного из ангеликового (дягильного) корня растения Angelica officinalis. А тиглиновая – из того же масла Croton tiglium, что и кротоновая кислота, только названа по второй части этого ботанического термина. Другой способ придумать новое название – переставить буквы в уже известном (такой пример будет приведен ниже). Сорбиновая (2,4-гексадиеновая) кислота СН3–СН=СН–СН=СНСООН была получена из ягод рябины (на латыни – sorbus). Эта кислота – прекрасный консервант, поэтому ягоды рябины не плесневеют. Названия цитронелловой (СН3)2С=СН–(СН2)2–СН(СН3)–СН2–СООН и гераниевой (СН3)2С=СН–(СН2)2–С(СН3)=СН–СООН кислот не требуют пояснений, чего нельзя сказать об изомерных непредельных кислотах состава С21Н41СООН – брассидиновой и эруковой. Эруковая кислота была выделена из масла растения Eruca – того же семейства Brassica, что и капуста, а также из масла репы (Brassica napus). При длительном нагревании с сернистой кислотой эруковая кислота изомеризуется в брассидиновую; интересно, что статья, в которой описана эта реакция, была подписана М.М.Зайцевым, К.М.Зайцевым, и А.М.Зайцевым (последний, Александр Михайлович, широко известен как автор «правила Зайцева»). Таририновая кислота с ацетиленовой связью СН3–(СН2)10–СС–(СН2)4–СООН была выделена из горького экстракта коры американского тропического дерева рода Tariri antidesma. Это крайне редкий случай нахождения в природе соединения с тройной связью. Высокомолекулярные непредельные кислоты часто упоминаются диетологами (они называют их ненасыщенными). Самая распространенная из них – олеиновая СН3–(СН2)7–СН=СН–(СН2)7–СООН (С18Н34О2). Изомерна ей кислота элаидиновая. Особенно важны полиненасыщенные кислоты с несколькими двойными связями: линолевая СН3–(СН2)4–(СН=СН–СН2)2–(СН2)6–СООН (С18Н32О2) с двумя двойными связями, линоленовая СН3–СН2–(СН=СН–СН2)3–(СН2)6–СООН (С18Н30О2) с тремя двойными связями и арахидоновая СН3–(СН2)4–(СН=СН–СН2)4–(СН2)2–СООН (С20Н32О2) с четырьмя двойными связями; их часто называют незаменимыми жирными кислотами. Именно эти кислоты обладают наибольшей биологической активностью: они участвуют в переносе и обмене холестерина, синтезе простагландинов и других жизненно важных веществ, поддерживают структуру клеточных мембран, необходимы для работы зрительного аппарата и нервной системы, влияют на иммунитет. Отсутствие в пище этих кислот тормозит рост животных, угнетает их репродуктивную функцию, вызывает различные заболевания. Линолевую и линоленовую кислоты организм человека сам синтезировать не может и должен получать их готовыми с пищей (как витамины). Для синтеза же арахидоновой кислоты в организме необходима линолевая кислота. Природные кислоты представлены в основном цис-изомерами. Некоторое время велась дискуссия о том, опасны ли транс-изомеры, которые ведут себя иначе; как выяснилось, в природных источниках их содержание невелико и не представляет опасности для человека. Полиненасыщенные жирные кислоты с 18 атомами углерода в виде эфиров глицерина находятся в так называемых высыхающих маслах – льняном, конопляном, маковом и др. В названиях олеиновой, элаидиновой, линолевой, линоленовой кислот легко усмотреть «масло» (греч. elaion, лат. oleum) и «лён» (лат linum); в льняном масле содержится до 30% линолевой и до 60% линоленовой кислот, а название арахидоновой (как и арахиновой) происходит от арахиса. С анализом российского рынка жирных кислот Вы можете познакомиться в отчете Академии Конъюнктуры Промышленных Рынков «Рынок жирных кислот в России».
www.newchemistry.ru
|
