КОНТРОЛЬ СОДЕРЖАНИЯ ДИОКСИНОВ В ОРГАНИЗМЕ ЧЕЛОВЕКА
Группа веществ, называемых «диоксинами», регулярно оказывается в центре внимания общественности.

В последний раз это произошло в 2010 г, когда в организме рабочих одного из предприятий в Дортмунде, занимающегося переработкой отработанных трансформаторов, были обнажены ПХБ и диоксины высокой концентрации, этом же году стало известно о том, что содержащий примеси диоксина жир входил в состав корма для животных, которых люди употребляют в пищу, что вызвало резонанс в масштабах всей страны, заставив потребителей, фермеров, органы власти и политиков на несколько
недель затаить дыхание.
Биомониторинг - контроль содержания вредных веществ и продуктов их метаболизма в организме человека, а также, в более широком смысле, их биохимического к биологического вреда - хорошо подходит для оценки степени воздействия и риска. В начале 1990-х в крови людей и женском грудном молоке были обнаружены следовые количества диоксинов.
Диоксин - что это?
Полихлорированные дибензо-р-диоксины (ПХДД) и дибензофураны (ПХДФ), часто сокращенно называемые «диоксинами», относятся к классу хлорсодержащих ароматических эфиров и диэфиров. По структуре различают 75 отдельных соединений (конгенеров) ПХДД и, соответственно, 135 -ПХДФ, отличающиеся друг от друга числом а юмов хлора, а также их расположением друг относительно друга. ПХДД/Ф обозначают в соответствии с замещающими атомами хлора или систематической нумерацией ИЮПАК. Из большой группы этих очень сходных по строению соединений непосредственно токсичны только те семь ПХДД и десеять ПХДФ, в которых замещающие атомы хлора имеются как минимум в положениях 2, 3, 7 и 8. Наряду с этим существуют четыре полихлорированпых бифенила (ПХБ) с заместителями не в орто-положениях и восемь моно-ортозамещенных ПХБ, обладающих сходным токсическим действием вследствие структурного сходства с ПХДД и называемых диоксиноподобными ПХБ (см. рис. 1).
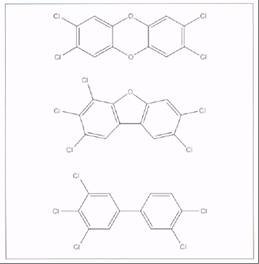
Рис. 1 Структурные формулы
2.3,7,8-тетрахлоридбензо-р-диоксина
2,3,4,7,8-пснтахлоридбензофурана и
3,3',4,4',5-пентахлорбифенила (# 126)
Эквиваленты токсичности
Действие отдельных ПХДД/Ф-конгенеров и диоксиноподобных соединений очень сильно варьирует. Для грубой оценки риска, связанного с воздействием сложных смесей ПХДД/Ф и ПХБ, была разработана концепция эквивалентов токсичности. Эта концепция исходит из сходного и аддитивного действия веществ и основана преимущественно на результатах исследований ферментативной индукции, острой токсичности, канцерогенности и репродуктивной токсичности. Каждому соединению соответствует так называемый коэффициент эквивалентной токсичности (ОТ), служащий мерой токсичности данною вещества по отношению к токсичности 2,3,7,8-тетраХДД, при этом для оценки токсичности последнего используют коэффициент 1. Умножая количество вещества на соответствующий ОТ и складывая взвешенные значения, можно выразить количество вещества через силу токсического действия, равную токсическому действию соответствующего количества 2.3,7,8-те-траХХД. Рассчитанные значения обозначают как токсические эквиваленты (ТЭ).
Исторический обзор
Промышленное электрохимическое производство хлора стало возможным в конце 19-го века, когда появились необходимые для этого генераторы. В это же время хлор начали применять в промышленности, и возникло первое производство хлорорганических соединений. Довольно скоро стало очевидным исключительно вредное воздействие хлорорганических соединений на организм человека. Так в 1899 г впервые была описана картина хлорною акне заболевания рабочих, занятых на электрохимическом производстве хлора. Тогда подобного рода случаи наблюдались часто, однако их причина оставалась неясной. Теперь уже известно, что заболевание обусловлено не самим хлором, а содержащими его соединениями и их накоплением в организме. Судя по тому, что заболевание развивается у членов семьи больного, не имевших непосредственного контакта с вредными веществами, последние способны переноситься.
После второй мировой войны были описаны многочисленные случаи хлорного
акне в результате воздействия хлорсодержащих соединений па рабочем месте. Однако часто такие случаи не предавались гласности. Взаимосвязь между 2,3,7,8-тетраХДД и хлорным акне или токсичностью хлорсодержащею диоксина стала очевидной только в середине 1950-х гг.
Всплеск общественного внимания к диоксину возник в связи с распылением американскими войсками дефолианта «Agent Orange» (Агент Оранж), содержащего 2,3,7,8-тетраХДД, в ходе операции «Ranch Hand» во Вьетнаме с 1962 по 1970 гг. Из-за употребления рисового масла, загрязненного преимущественно ПХБ и ПХДФ. в 1968 г в Японии более 1800 человек стали жертвами заболевания, получившего название болезни Юшо («масляной болезни»). И, наконец, в 1976 г в компании ICMESA в Ссвсзо, Северная Италия, произошла катастрофа, получившая всемирную известность: из-за выхода из-под контроля процесса синтеза трихлорфенола в атмосферу было выброшено более 2 кг 2,3.7.8- тетраХХД
Ситуация с загрязнением в настоящее время
В настоящее время в индустриальных странах Запада дальнейшее поступление хлор-содержащих соединений в окружающую среду незначительно, однако их накопленные остатки могут иметь значительные последствия. Важными первичными источниками ПХДД/Ф в воздухе являются литейные и металлообрабатывающие производства, заводы по сжиганию отходов, предприятия, сжигающие топливо, а также сжигание топлива для бытовых нужд.
Из-за повсеместного распространения ПХДД/Ф они в незначительных концентрациях присутствуют в различных средах, воздействуя на население в целом, причем степень вреда зависит от пути поступления в организм: оральный ингаляционный -чрескожный (в порядке уменьшения значимости). ПХДД/Ф способны накапливаться в пищевой цепи, при этом наибольшее значение имеют следующие цепи; «воздух —∙ наземные растения —наземные животные —человек» и «вода —» водные организмы —∙человек». При этом почти всегда избирательно накапливаются конгенеры с замещающими атомами хлора в положениях 2, 3, 7, 8. Основным источником попадания этих веществ в организм вследствие фонового загрязнения окружающей среды является употребление в пищу продуктов животного происхождения.
Методы анализа
Анализ проб крови на диоксины включает следующие стадии: экстракция, очистка, газохроматографическое разделение и качественное и количественное определение с помощью масоспектрометрии. При этом самой трудоемкой стадией является выделение диоксина из материала пробы. На этой стадии необходимо полностью отделить содержащиеся в следовой концентрации анализируемые соединения от мешающих анализу веществ, таких как липиды и другие компоненты человеческой крови. Это осуществляют с помощью нескольких согласованных стадий разделения хроматографией на колонках с модифицированным силикагелем и активированным углем. В конечном итоге молекулы, содержащиеся в исходной пробе цельной крови объемом 50 мл, концентрируют в нескольких микролитрах.
Затем полученный экстракт анализируют с помощью капиллярной газовой хроматографии (КГХ) и масоспектрометрии высокого разрешения (МСВР). Газовая хроматография позволяет почти полностью разделить 210 различных конгенеров па основании их температуры кипения и структурных свойств. После хроматографического разделения, продолжающегося около часа, продукты поступают- в масс-спектрометр, где ионизируются, ускоряются в магнитном поле и разделяются по массе. Затем происходит регистрация ионов, сигнал переводится в цифровую форму и записывается подсоединенной компьютерной системой.
«Диоксины» идентифицируют по времени удержания в газовом хроматографе, а также по соотношению изотопов нескольких характерных масс. Для количественного определения силу сигнала этих фрагментов сравнивают с силой сигнала меченых изотопом «диоксинов», известное количество которых было добавлено к образцу крови перед анализом. После этого в результат определения концентрации обычно вносят поправку на липиды или объем крови и представляют его в виде численного значении. Mace-спектрометрия высокого разрешения позволяет определять крайне низкие концентрации диоксинов — менее 1 пг (0.000000000001 г) на грамм липидов крови.
Характер и тенденции фонового загрязнения
Из-за длительного периода полувыведен и; диоксинов- до нескольких лет-их непрерывное поступление с пищей даже в самых низких концентрациях приводит к накоплению в человеческом организме с характерной картиной аккумуляции отдельных конгенеров. В крови людей обнаруживают почти исключительно соединения с замещающими атомами хлора в положениях 2. 3, 7, 8. Конпентраци: ПХДД возрастает с увеличением числа атомом хлора в молекуле, а в случае ПХДФ - снижается от пентаХДФ к октаХДФ. Основных компонентом является октаХДД.
С возрастом концентрация различны конгенеров растем поэтому содержание диоксинов в крови пожилых людей явно выше чем у молодых (см. рис. 2). К этому следует добавить, что благодаря мерам снижению выбросов в Германии в последние годы концентрация этих веществ в окружающей ере де сильно уменьшилась, что также отражается на их содержании в организме людей. Например, из рис. 3 видно, что за последни 20 лет концентрация диоксина в грудном молоке снизилась примерно на 80%.
Таким образом, индивидуальная оцени концентрации диоксина в крови возможна только с учетом момента проведена исследования и возраста человека. Как и случае с другими параметрами, значимым считаются концентрации диоксина, которые в пересчете на суммарный параметр ТЭ или концентрации отдельных конгенеров превышают 95-й процентиль фонового загрязнения. Вариации состава конгенеров часто бывают типичными для той или иной формы воздействия, позволяя в точности, как на основании отпечатков пальцев, сделать заключение об источнике поступления этих веществ.
Факторы, влияющие на фоновое загрязнение
В зависимости от того, где произошел контакт с диоксинами на рабочем месте или в результате загрязнения помещения (основные источники: средства защиты древесины, длительно сохраняющие эластичность герметики и т. п.), воздействие при этом оказывают определенные, как правило, одни и те же факторы. В первую очередь это - характер питания. Однако значительную роль могут играть и другие факторы. Например, грудное вскармливание в определенной степени приводит к удалению вредных веществ из организма матери с молоком и, одновременно, переходу их в организм младенца. Снижение содержания ПХДД/Ф и ПХБ в организме матери сопровождается снижением концентрации этих веществ у нее в крови (см. рис. 2). К прочим факторам, достойным упоминания, относятся курение, индекс массы тела, колебания массы тела, собственно поступление с молоком (см. выше), а также поступление и окружающей среды (материалов жилища).
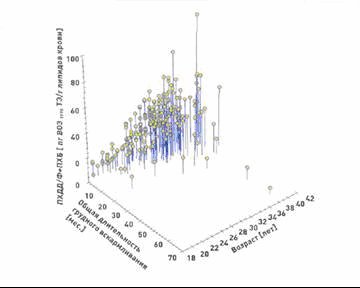
Рис.2 Влияние возраста и кормления грудью на содержание ПХДД/Ф и ПХБ в крови
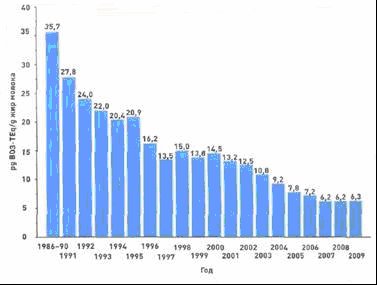
Рис.3 Тенденция изменения содержания диоксинов со временем
Источник: журнал «Labor&more»