ОБЗОР ТЕХНОЛОГИЙ ПРОИЗВОДСТВА ДИОКСИДА ТИТАНА
Пигменты диоксида титана существует в двух формах – анатазная и рутильная и производятся по двум технологическим схемам: сульфатный и хлорный способы.

Обе, анатазная и рутильная формы диоксида титана, могут быть произведены любым из способов. Сульфатный способ был внедрен в промышленность в 1931 г., для производства анатазной формы диоксида титана, а позже, в 1941 г. – рутильной. В этом способе руда, содержащая титан (ильменит и др.), растворяется в серной кислоте, образуя растворы сульфатов титана, железа и других металлов. Затем, в ряде химических реакций, включающих в себя химическое восстановление, очистку, осаждение, промывание и кальцинацию, образовывая базовый диоксид титана с необходимым размером частиц. Строение кристаллов (анатазная или рутильная форма) контролируется в процессе ядрообразования и кальцинации.
Хлорный способ был изобретен компанией DuPont в 1950 г. для производства рутильной формы диоксида титана. Этот способ включает в себя высокотемпературные фазовые реакции. Титансодержащая руда вступает в реакцию с хлорным газом при пониженном давлении, в результате чего образуется тетрахлорид титана TiCl4 и примеси хлоридов других металлов, которые впоследствии удаляются. TiCl4 высокой степени чистоты затем окисляют при высокой температуре, в результате чего образуется диоксид титана.
По сравнению с сульфатным хлоридный способ является более экологически чистым и совершенным благодаря возможности осуществлять процесс в непрерывном режиме, что предполагает полную автоматизации производства. Однако он избирателен к сырью, а в связи с использованием хлора и высоких температур требует применения коррозионностойкого оборудования.
Сульфатный метод
Технология производства состоит из трёх этапов:
(1) получение растворов сульфата титана (путём обработки ильменитовых концентратов[1] серной кислотой). В результате получают смесь сульфата титана и сульфатов железа (II) и (III), последний восстанавливают металлическим железом до степени окисления железа +2. После восстановления на барабанных вакуум-фильтрах отделяют растворов сульфатов от шлама. Сульфат железа(II) отделяют в вакуум-кристаллизаторе.
(2) гидролиз раствора сульфатных солей титана. Гидролиз проводят методом введения зародышей (их готовят осаждая Ti(OH)4 из растворов сульфата титана гидроксидом натрия). На этапе гидролиза образующиеся частицы гидролизата (гидратов диоксида титана) обладают высокой адсорбционной способностью, особенно по отношению к солям Fe3+, именно по этой причине на предыдущей стадии трёхвалентное железо восстанавливается до двухвалентного. Варьируя условия проведения гидролиза (концентрацию, длительность стадий, количество зародышей, кислотность и т. п.) можно добиться выхода частиц гидролизата с заданными свойствами, в зависимости от предполагаемого применения.
(3) термообработка гидратов диоксида титана. На этом этапе, варьируя температуру сушки и используя добавки (такие, как оксид цинка, хлорид титана и используя другие методы можно провести рутилизацию (то есть перестройку оксида титана в рутильную модификацию). Для термообработки используют вращающиеся барабанные печи длиной 40—60 м. При термообработке испаряется вода (гидроксид титана и гидраты оксида титана переходят в форму диоксида титана), а также диоксид серы.
Производство диоксида титана сульфатным методом
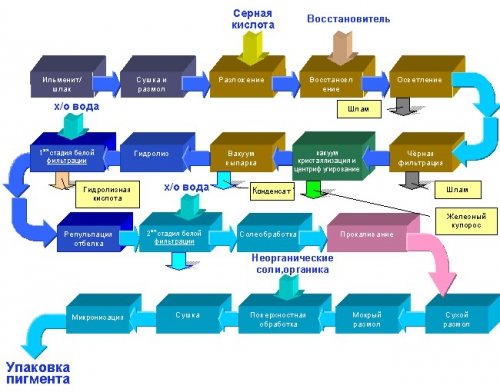
Известны три варианта периодического процесса разложения ильменита серной кислотой — жидкофазный, среднефазный и твердофазный, различающиеся по концентрации используемой серной кислоты и характеру образующихся продуктов разложения. Однако в промышленной практике наибольшее применение получил твердофазный метод, позволяющий наиболее быстро и полно вскрывать концентраты и получать растворы большей основности, что облегчает проведение I гидролиза и получение готового продукта повышенного качества.
Для разложения ильменита по данному методы применяют концентрированную серную кислоту, благодаря чему температуру реакционной смеси можно быстро довести до 190—220 °С (резко повысить температуру удается добавлением к концентрированной кислоте воды или гидролизной кислоты), что обеспечивает быстрое протекание процесса и высокую степень разложения концентрата — 96-97%. После выщелачивания получаемые растворы сульфата титана имеют низкий (~1,8) кислотный фактор. Кроме периодического существуют и непрерывный способы разложения ильменита.
Гидролиз в целях его ускорения и улучшения качества (дисперсности) получаемых гидратов ведут кипячением в присутствии затравки (зародышей) из растворов сульфата титана с концентрацией TiO2 не менее 190—200 г/л при кислотном факторе >2. Не приводя здесь технологический режим гидролиза и механизм процесса, который сложен, отметим, что при этой операции, протекающей по суммарному уравнению
образуется большое количество (в пересчете на моногидрат ~2 т на 1 т ТiO2) разбавленной 2%—22%-ной гидролизной серной кислоты, загрязненной сульфатом железа, 1—2% титанилсульфата и несколькими процентами других сульфатов. Эта кислота является отходом производства, однако возврат ее затруднен. Возможное направление утилизации гидролизной кислоты - упаривание до концентрации 55% с последующим ее использованием для производства суперфосфата.
При гидролизе в осадок выделяется до 95—96% титана, причем образующаяся метатитановая кислота сорбирует значительное количество SО3. Метатитановую кислоту затем промывают, сушат и прокаливают, в результате чего из нее удаляется вначале вода (при 200-300 °С), затем SО3 (при 500-800 °С) и при 850-900 °С получается нейтральный (рН 7) продукт - диоксид титана.
Побочный продукт производства (семиводный железный купорос) прокаливают до получения одноводного (FeSО4 · Н2О) и измельчают.
Примерный расход основных материалов на производство из ильменитовых концентратов сернокислотным методом 1 т диоксида титана составляет, т: ильменитового концентрата, содержащего 42% TiO2 -3,1; серной кислоты (моногидрат) — 4,0—4,5; железной стружки — 0,24.
Как указано выше, источником для получения TiO2 могут служить также получаемые при рудовосстановительной плавке ильменитовых концентратов титановые шлаки. На шлаках (70% TiO2), в частности, работает завод большой производительности в Канаде (провинция Квебек, близ Сореля).
При получении диоксида титана из шлаков сернокислотным методом растворы после выщелачивания сульфата титана, содержащие 190 г/л TiO2 и малое количество железа, гидролизуются легче, чем при переработке ильменитовых концентратов. Получаемая гидролизная кислота содержит ~9 г/л железа, что облегчает ее регенерацию.
Сернокислотный метод производства диоксида титана из ильменита и титановых шлаков имеет ряд существенных недостатков — сложная многостадийная схема, высокий расход серной кислоты, значительное количество которой непроизводительно расходуется на образование больших количеств отходов — сульфата железа (>3 т семиводного продукта на 1 т TiO2), а также разбавленной 20—22%-ной и загрязненной примесями гидролизной серной кислоты. По этой причине в настоящее время все большее значение приобретает другой — хлорный метод.
Хлорный метод
Хлорный метод получения диоксида титана заключается в том, что исходным сырьем (полуфабрикатом) служит тетрахлорид титана. Из него диоксид титана можно получать методом гидролиза или сжиганием при высокой температуре. Тетрахлорид титана гидролизуется при нагревании водных растворов, либо в газовой фазе под действием паров воды.
Промышленные методы производства титановых пигментов методом гидролиза еще не разработаны. Общий недостаток их — неудовлетворительное решение проблемы использования образующихся при гидролизе хлорида водорода или соляной кислоты, которые не удается вернуть для повторного использования в производстве диоксида титана.
Гидролиз тетрахлорида титана парами воды при 25—75 °С на воздухе приводит к образованию вязкой жидкости, затвердевающий при Длительной выдержке в белую массу. Парофазный гидролиз при 1000-1200 °С позволяет получать диоксид титана с пигментными свойствами, поэтому его можно использовать при условии нахождения эффективного метода утилизации хлорида водорода.
Сжигание тетрахлорида титана кислородом протекает по реакции:
TiCl4 + O2= TiO2 + 2С12.
Выделяющийся хлор может быть возвращен в производство для получения тетрахлорида титана, поэтому метод сжигания уже применяют в промышленном производстве. Важнейшей операцией в производстве пигментного диоксида титана хлорным методом является сжигание тетрахлорида титана. Оно производится при 900—1000 °С на горелках специальной конструкции, обеспечивающих поддержание температуры реакции в заданных пределах и выдерживание продуктов сгорания в течение определенного времени.
Для получения монодисперсного продукта пребывание диоксида титана в зоне высоких температур не должно превышать 0,01—5 с. В зависимости от условий сжигания тетрахлорида титана диоксид титана имеет структуру рутила или анатаза. Смешение исходных реагентов при 400 °С приводит к образованию анатаза с размером частиц 0,5—1,0 мкм. Предварительное нагревание их до 1000 °С при сжигании дает продукт, содержащий до 60% рутила. Сжигание тетрахлорида титана с примесью тетрахлорида кремния (0,5—4,0%) приводит к уменьшению размеров частиц диоксида титана. Тетрахлорид кремния способствует также снижению так называемой фотоактивности диоксида титана. Добавка к продуктам сжигания еще и хлорида алюминия (1—5%) ускоряет переход анатаза в рутил. Доля рутила в готовом продукте зависит от концентрации зародышевых кристаллов, возникающих на первой стадии реакции.
Титановые пигменты, получаемые при сжигании тетрахлорида титана, содержат до 0,6% адсорбированного хлора. Водная суспензия такого продукта имеет рН>7, и он не пригоден для приготовления красок. Десорбцию хлора из пигмента можно осуществить прокаливанием его при 300-900 °С, примесь хлора при этом понижается до 0,1%. Такой продукт имеет рН водной вытяжки 5-6,8 и пригоден для изготовления красок и эмалей, но нуждается в поверхностной обработке соединениями кремния и алюминия.
Получение диоксида титана из сфенового концентрата
В последнее время разработан и опробован ряд новых вариантов технологии, предусматривающих получение пигментных продуктов из сфена.
В данном варианте твердую фазу суспензии отделяют от жидкой до наступления момента осаждения из нее соли титана. При этом в осадке остаются сульфат кальция, кремнезем (SiO2) и неразложившиеся минералы, а жидкая фаза представляет собой титансодержащий раствор, пригодный для прямого выделения титановой соли – TiOSО4 · Н2О. При термогидролизе раствора СТМ получается пигментный диоксид титана рутильной модификации высших марок. Переработка титановой соли TiOSО4 · Н2О может быть организована на месте ее получения. Титановую соль можно транспортировать с целью переработки и в другие районы. Маточный раствор после выделения соли полностью возвращается на сульфатизацию, вследствие чего существенно снижается расход серной кислоты (до 3,5—4,5 т на 1 т диоксида титана).
Принципиальная схема переработки сфенового концентрата
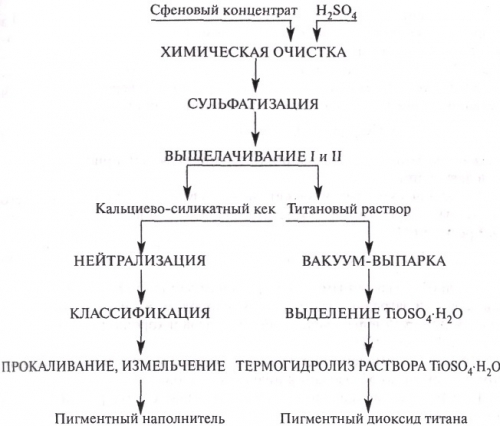
Источник: Тарасов А.В. Металлургия титана. М., 2003.
[1]Ильменит - это руда, которая с химической точки зрения представляет собой смесь оксидов, большую часть из которых составляют оксиды титана и железа. Сульфатная технология производства двуокиси титана основана на обработке ильменита серной кислотой