ОБЗОР ТЕХНОЛОГИЙ ПРОИЗВОДСТВА АНИЛИНА
Производство анилина в промышленном масштабе было организовано в 1866 г. шотландским химиком А. Купером. Анилин получали из очищенного нитробензола по схеме А. Бешана.

В 1872 г. русским ученым М.М. Зайцевым была открыта реакция восстановления нитросоединений водородом в присутствии катализаторов. Превращение нитробензола в анилин было осуществлено путем пропускания смеси паров нитробензола и водорода над палладиевой чернью, помещенной в нагретую до 150 °С стеклянную трубку.
В начале XX в. французские химики П. Сабатье и Ж. Сандеран показали, что и многие другие металлы, имеющие большую удельную поверхность, например получаемые восстановлением их оксидов при нагревании в струе водорода, оказываются эффективными катализаторами восстановления нитробензола в анилин. Однако прежде чем процесс газофазного восстановления нитробензола был реализован в промышленности, прошло около 50 лет. С середины 1950-х гг. получение анилина каталитическим восстановлением нитробензола водородом занимает прочное место среди промышленных методов синтеза анилина, а к началу 1960-х гг. этот способ почти повсеместно вытесняет другие методы.
В незначительных количествах анилин содержится в каменноугольной смоле.
Методы получения анилина
Восстановление нитробензола
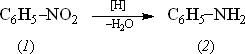
Это самый распространенный метод получения анилина. В качестве восстановителей могут быть использованы самые разнообразные неорганические и органические вещества. Применение в технике нашли соединения, наиболее доступные по цене и удобные для практического использования: металлы (железо, цинк, олово), соли (хлорид олова, сульфиды щелочных металлов, гидросульфиты), сероводород. Кроме того, восстановление можно вести каталитическим или электрохимическим методом. В лабораторной, а в последние годы — и в заводской практике все большее значение приобретает восстановление нитробензола смешанными гидридами металлов: алюмогидридом лития, боргидридом натрия.
Восстановление нитросоединений протекает ступенчато и в общем виде может быть выражено уравнением (4.2.1).
Конечный продукт реакции зависит от природы восстановителя и характера среды. В кислой среде конечным продуктом восстановления всегда является анилин (2), а нитрозобензол (3) и фенилгидроксиламин (4) образуются в качестве промежуточных продуктов. Однако в нейтральной среде нитрозобензол и фенилгидроксиламин могут быть получены как конечные продукты восстановления нитробензола. В щелочной среде процесс идет более сложно (уравнение (4.2.2)), т. к. фенилгидроксиламин (4), являясь весьма реакционноспособным соединением, в этих условиях активно взаимодействует с нитро- (1) или нитрозобензолом (3), образуя азоксибензол (5). При дальнейшем восстановлении азоксибензол превращается в азобензол (6), далее в гидразобензол (7) и, наконец, в анилин.
Обычно восстановление нитробензола металлами и их солями в щелочной среде приводит к образованию азобензола (SnCl2; NaOH) или гидразобензола (Zn; NaOH); анилин в этих условиях не получают. Однако при восстановлении нитробензола в щелочной среде сульфидами щелочных металлов образуется анилин. Таким образом, варьируя восстановитель и условия восстановления, можно регулировать процесс, получая тот или иной целевой продукт.
Восстановление нитробензола железом в присутствии электролитов
В 1854 г. французским химиком Антуаном Бешаном была открыта реакция восстановления нитробензола железом в слабокислой среде. Этот метод получения анилина, известный как метод Бешана, оказался простым и доступным. Как промышленный метод получения анилина он существует с 1856 г. Достоинствами этого метода являются высокий выход анилина, отсутствие побочных продуктов, дешевизна восстанавливающего агента и простота технологического оформления процесса.
Механизм восстановления нитросоединений железом, в частности чугунными стружками, был обстоятельно изучен В.О. Лукашевичем, который показал, что реакция протекает в две стадии. На первой стадии происходит восстановление нитросоединения железом, при этом железо окисляется и образуется гидроксид железа(II) (уравнение (4.2.3)). Гидроксид железа(II) также способен восстанавливать нитросоеди¬нение до амина, превращаясь при этом в гидроксид железа(III) (уравнение (4.2.4)). Реакция идет с большой скоростью.
Соотношение скоростей первой и второй стадий определяет соотношение в реакционном шламе оксидов железа, образующихся из гидроксидов путем дегидратации. На соотношение образующихся оксидов железа влияет также наличие избытка чугунной стружки (уравнение (4.2.5)), степень ее измельчения и природа применяемого электролита. При восстановлении в присутствии хлорида аммония, например, в шламе содержится 49,7 % оксида железа (III), а в присутствии хлорида железа (III) содержание оксида железа (III) составляет 74,7 %.
С6Н5NO2 + 3Fe + 4H2O → С6Н5NH2 + 3Fe(OH)2 | (4.2.3) |
| С6Н5NO2 + 6Fe(OH)2 + 4H2O → С6Н5NH2 + 6Fe(OH)3 | (4.2.4) |
| Fe + 8Fe(OH)3 → 3Fe3O4 + 12H2O | (4.2.5) |
Суммарном уравнением реакции восстановления ароматических нитросоединений железом в присутствии электролитов является уравнение (4.2.6).
4С6Н5NO2 + 9Fe + 4H2O → 4С6Н5NH2 + 3Fe3O4 | (4.2.6) |
Как видно из приведенных уравнений, восстановление протекает только за счет железа и воды. Однако чтобы реакция шла успешно, необходимо обеспечить условия влажной коррозии железа. Такие условия создаются при наличии в реакционной массе электролитов. В качестве электролитов применяют растворимые соли железа (хлорид, ацетат, формиат), соли аммония (сульфат, хлорид), реже хлорид натрия и сульфат железа (II).
Было показано, что скорость коррозии железа, которая в растворах солей в несколько раз (до 10) больше, чем в воде, зависит от природы и концентрации электролита. Наивысшая скорость процесса наблюдается при использовании хлоридов аммония и железа(II), несколько меньшая — при использовании сульфата аммония. Количество применяемого электролита обычно составляет 0,1–0,2 моль / 1 моль нитробензола.
Электролиты вводят в реакционную массу готовыми или (чаще) получают в самом аппарате взаимодействием чугунных стружек с разбавленными кислотами: соляной, серной, уксусной, муравьиной.
Этот процесс носит название протравливания чугуна (железа) и производится обычно до добавления нитросоединения.
Для восстановления лучше всего использовать стружку серого чугуна — отход металлообрабатывающих заводов. Серый чугун по химической природе представляет собой железо, в котором растворен углерод, образующий обнаруживаемые в микроструктуре чугуна углеродсодержащие компоненты: феррит и перлит, а также графит. Кроме того, в чугуне в небольших количествах содержатся соединения других элементов: Mn, P, Si, S. Химическая неоднородность чугуна является причиной его активности в отношении окисления во влажной среде (влажная коррозия), т. к. обусловливает возможность возникновения элементарных гальванических пар, например, феррит—графит. Выделяющийся при этом на аноде кислород способствует окислению железа. Вследствие зернистого строения серого чугуна его стружка очень хрупка и легко ломается, поэтому при размешивании в процессе восстановления она распадается на мелкие частицы. При этом значительно увеличивается ее поверхность соприкосновения с жидкостью, что ведет к ускорению восстановления. Часто перед употреблением стружку специально измельчают и просеивают.
Для восстановления нитробензола в анилин в промышленных масштабах были разработаны два способа: периодический и непрерывный.
Периодический способ. Восстановление нитробензола в анилин в аппаратах периодического действия осуществляется в промышленном масштабе более 100 лет без существенных усовершенствований (рис. 4.2.1).
Для восстановления нитробензола применяют цилиндрические реакционные аппараты (редукторы), стальные или чугунные, емкостью 10–20 м3, защищенные изнутри от коррозии и истирания кислотоупорной плиткой. Аппараты снабжены мощными тихоходными мешалками, необходимыми для размешивания тяжелого осадка, состоящего из чугунных стружек и оксидов железа. Через полый вал мешалки в аппарат подают острый пар для нагрева массы в начальный период восстановления. Редукторы некоторых конструкций имеют паровую рубашку для обогрева.
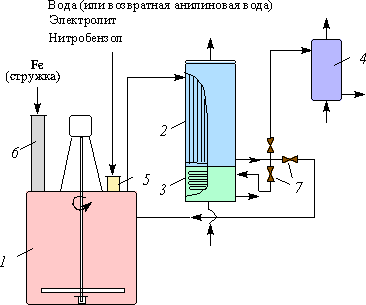
Рис. 4.2.1. Схема установки для получения анилина восстановлением нитробензола:
1 — редуктор; 2 — трубчатый холодильник; 3 — змеевиковый холодильник; 4 — холодильник для легких углеводородов;
5 — штуцер для загрузки реагентов; 6 — труба для загрузки чугунных стружек; 7 — краны
Порядок загрузки реагентов может быть различным. Обычно сначала в аппарат загружают воду (или возвратную анилиновую воду) и часть чугунной стружки, нагревают острым паром и добавляют готовый электролит или кислоту для протравливания стружки. Затем постепенно порциями добавляют нитробензол и оставшееся количество чугунной стружки.
Восстановление нитробензола в анилин сопровождается выделением большого количества тепла (548 кДж/моль), поэтому реакционная масса в редукторе находится постоянно в состоянии кипения, которое поддерживается за счет теплоты реакции. При этом испаряется большое количество воды и образующегося анилина. Пары воды и анилина конденсируются в обратном холодильнике и возвращаются в редуктор. Отгоняющийся анилин содержит некоторое количество непрореагировавшего нитробензола. После окончания загрузки нитробензола проводят небольшую выдержку до полного восстановления. Конец реакции определяют по исчезновению окраски конденсата, возвращающегося в редуктор, или по концентрации образовавшегося анилина, которую определяют с помощью титрования нитритом натрия.
После нейтрализации реакционной массы анилин из смеси выделяют. Применяется несколько методов выделения: отгонка анилина из редуктора острым паром, вакуум-отгонка анилина из реакционной массы, сифонирование анилина из редуктора. Из-за сложности аппаратурного оформления первый и второй методы не нашли широкого применения. Наиболее распространенным является третий метод — сифонирование, основанный на том, что при комнатной температуре плотность анилина больше, чем воды, но уже при 71 °С его плотность меньше. Разность в плотностях еще больше увеличивается при добавлении в редуктор хлорида натрия. Анилин всплывает наверх и может быть отделен сифонированием. Около половины анилина остается в водном слое и железном шламе и отгоняется с острым паром. Так как анилин частично растворим в воде (~3 %), водный слой после отделения анилина вновь возвращают в процесс или экстрагируют нитробензолом. Общий выход анилина ~97 % от теоретического.
Образующийся в процессе реакции шлам состоит из смеси оксидов железа: FeO и Fe2O3. Его промывают, сушат и прокаливают, при этом получают искусственные железооксидные пигменты красного, коричневого и черного цветов. Если проводить восстановление в присутствии хлорида алюминия, образуется гидрат оксида железа FeО(OН) или Fe2O3 • H2O находящий применение в качестве желтого пигмента.
Этот промышленный метод восстановления нитросоединений до аминов практически потерял свое значение для анилина. В настоящее время он используется лишь для получения малотоннажных аминов: о- и п-толуидинов, ксилидинов, п-фенилендиамина, о-хлоранилина, 2,5-дихлоранилина.
Непрерывный способ. При непрерывном восстановлении нитробензола применяют редуктор той же конструкции, что и при периодическом. Для ускорения реакции восстановления в процесс вводят самый активный электролит — хлорид аммония и чугунную стружку, обладающую повышенной активностью, равномерно измельченную и очищенную от примесей.
Нитробензол, раствор хлорида аммония и «анилиновая вода» из напорных емкостей поступают в смеситель 1 (рис. 4.2.2), смешиваются там и насосом 2 подаются в редуктор 3 под слой чугунной стружки, которая непрерывно подается в редуктор шнековым питателем 4. Острым паром через барботер реакционную массу нагревают до кипения, а затем кипение поддерживается за счет теплоты реакции. Подача в редуктор нитробензола, раствора хлорида аммония, анилиновой воды, а также чугунной стружки регулируется автоматически. При постоянной подаче этих компонентов ход реакции зависит только от количества загружаемой в редуктор чугунной стружки, активность которой может в известных пределах колебаться.
Электродвигатели питателя и мешалки сблокированы. При избыточной загрузке редуктора стружкой возрастает потребляемая мощность электродвигателя мешалки. В этом случае автоматически временно прекращается подача стружки шнековым питателем.
Полнота реакции восстановления контролируется фотоколориметрически: остаточное содержание нитробензола не должно быть выше 0,05 %. При увеличении содержания нитробензола в анилине выше 0,05 % поток жидкости, вытекающей из конденсатора 5, автоматически с помощью исполнительных механизмов направляется в аварийные емкости, а подача реагентов в редуктор снижается.
Основное количество полученного анилина отгоняется из редуктора с водяным паром, часть которого образуется вследствие теплоты реакции, а часть подается в редуктор через барботер. Пары анилина и воды направляются в конденсатор 5. Шламовая жидкость, в которой остается более 40 % анилина, непрерывно удаляется из редуктора через верхний боковой штуцер и перетекает в аппарат 6, из которого острым паром отгоняют оставшийся анилин. Анилин и водяной пар конденсируются в аппарате 7, охлаждаемом водой. Конденсат попадает в отстойник шлама 8, холодильник 9 и сепаратор 10, в котором водный анилин отделяется от анилиновой воды.
Сырой анилин собирается в сборнике 11, из которого подается на вакуум-перегонку для получения товарного продукта. Анилиновая вода собирается в сборнике 12, а затем перегоняется в насадочной колонне. Разбавленная анилиновая вода после охлаждения возвращается в редуктор, а смесь анилина с водой — в сепаратор 10. Если баланс анилиновой воды почему-либо нарушился, то перед сбросом ее в канализацию анилин экстрагируют нитробензолом.
Непрерывный способ восстановления нитробензола чугунной стружкой в среде электролита впервые был разработан и внедрен в промышленность в Советском Союзе.
Этот метод позволил несколько улучшить условия труда, но технико-экономические показатели производства существенно не улучшились. Непрерывный метод используется до сих пор, хотя и он фактически утратил свое значение из-за большого количества сточных вод, содержащих анилин и нитробензол, громоздкости аппаратуры и трудоемкости. Важной проблемой является также утилизация образующегося железного шлама.
Каталитическое восстановление нитробензола
В настоящее время этот способ восстановления нитробензола с целью получения анилина в промышленности является основным, т. к. отличается высокой скоростью, чистотой получаемых продуктов, простотой технологии, возможностью автоматизации технологического процесса.
Направление реакции и степень восстановления нитросоединения часто зависят от условий процесса и природы применяемых катализаторов. Роль катализатора в процессах каталитического восстановления заключается в активации реагентов — восстанавливаемого соединения и молекулярного водорода. При сорбции водорода на активных центрах катализатора (К) ослабляются или даже полностью разрываются химические связи в молекулах водорода (уравнение (4.2.7)).
К + Н2 → К···Н2 → К–Н···Н → 2К–Н | (4.2.7) |
Нитросоединения также сорбируются на катализаторе, но в меньшей степени. Дальнейшее взаимодействие происходит между двумя сорбированными молекулами, находящимися на соседних активных центрах. При этом образуется продукт гидрирования, обладающий меньшей сорбционной способностью, вследствие чего он вытесняется с активных центров катализатора новой молекулой нитросоединения.
Активность катализаторов, применяемых в реакциях гидрирования нитросоединений, зависит от их химического состава и физического состояния. Чаще всего применяются металлические катализаторы, особенно металлы VIII группы периодической системы — платина, палладий, родий, никель, кобальт, а также сплавы никеля и хрома, никеля и меди и др. Показано, что активность катализатора увеличивается, если он содержит примеси некоторых веществ — загрязнения или же специальные добавки — так называемые активаторы. Большое значение имеет также степень измельчения катализатора. Максимальное раздробление достигается осаждением каталитически активного вещества на так называемый носитель.
Роль активаторов и носителей до настоящего времени полностью не выяснена. Известно, что те и другие вызывают изменения структуры поверхности катализатора, носители, кроме того, значительно увеличивают поверхность катализатора. В результате уменьшается склонность катализатора к спеканию при повышенных температурах. Вероятно, добавление активатора или носителя увеличивает количество активных центров, а также их характер. В качестве активаторов применяются чаще всего оксиды и гидроксиды различных металлов, реже некоторые их соли, причем для каждой пары катализатор—активатор существует оптимальное количественное соотношение, при котором катализатор имеет максимальную активность.
В качестве носителей применяют различные пористые материалы, такие, как активированный уголь, асбест, пемза.
Способ приготовления катализаторов оказывает огромное влияние на их активность и область применения. Чувствительность катализаторов к небольшим изменениям условий их получения очень велика, вследствие чего даже катализаторы, полученные, казалось бы, при одинаковых условиях, обычно обнаруживают различную активность.
Реакция восстановления нитросоединений водородом идет по уравнению (4.2.8).
Реакция, как видно из уравнения, идет с уменьшением объема. Поэтому ее проводят при сравнительно низкой температуре и преимущественно под давлением.
Каталитическое восстановление нитробензола проводят в паровой или жидкой фазе.
| (4.2.8) |
Восстановление в паровой фазе.
В условиях парофазного процесса нитросоединение испаряется, смешивается с избытком водорода и пропускается через контактный аппарат, заполненный твердым катализатором. Процесс восстановления идет на поверхности катализатора до полного превращения нитросоединения в амин. Реакционное тепло отводится либо избытком водорода, либо высококипящим органическим теплоносителем (ВОТ). Реакционные газы охлаждаются, амин конденсируется, а избыток водорода возвращается в цикл. Преимущество метода в том, что катализатор не увлекается реакционными газами.
Катализаторами этого процесса являются активные сплавы никеля, алюминия, вольфрама, медь, нанесенная на оксид кремния. Наиболее подходящим катализатором для восстановления нитробензола является медь, т. к. ее действие распространяется только на нитрогруппу, не затрагивая ароматического ядра. В присутствии медного катализатора превращение нитробензола в анилин начинается при 230 °С, между 300 и 400 °С реакция проходит быстро. При избытке водорода выход анилина достигает 98 %, причем в получаемом продукте содержатся лишь следы азобензола. Водород может быть заменен водяным газом (смесь СО и Н2О), при этом монооксид углерода также играет роль восстановителя, превращаясь в диоксид.
Медь, полученная восстановлением гидроксида меди (II), более активна как катализатор восстановления, чем полученная из нитрата меди (II). Медь, нанесенная на асбест, более активна, чем нанесенная на пемзу или приготовленная без носителя. Однако медь, нанесенная на асбест, скорее теряет активность.
В промышленности катализатором служит карбонат меди, нанесенный в виде суспензии в растворе силиката натрия на пемзу и восстановленный водородом. Катализатор хорошо работает около года, но за этот период дважды подвергается регенерации.
Схема производства анилина каталитическим восстановлением нитробензола в паровой фазе изображена на рис. 4.2.3.
Нитробензол из резервуара проходит через экстрактор, в котором извлекает полученный анилин из воды, образующейся в результате реакции, и поступает в напорный бачок 6, а затем в трубчатый испаритель 5. Испарение нитробензола происходит в тонкой пленке, нагрев осуществляется горячим водородом, нагнетаемым газодувкой 2 и проходящим через теплообменники 3 и 4. Пары нитробензола смешиваются с водородом и проходят в два соединенных последовательно контактных аппарата 7 и 8 (конвекторы), содержащих катализатор. В качестве катализатора наиболее часто используют медь на носителях, т. к. при использовании этих катализаторов не идет гидрирование ароматического кольца. Реакция начинается в первом аппарате при 170 °С, при выходе из второго аппарата температура смеси доходит до 350–370 °С. Давление в аппаратах 0,15–0,20 МПа.
Из реакторов контактные газы проходят через теплообменник 3, нагревая водород, а затем поступают в конденсатор 9, где конденсируются пары анилина и воды. Для полного улавливания анилина газы проходят через теплообменник 10 с развитой охлаждающей поверхностью и сепаратор 11. Избыток водорода возвращается в цикл, конденсат стекает в отстойник 12, из которого «анилиновая вода» поступает на экстракцию нитробензолом, а анилин — на вакуум-перегонку. Выход анилина составляет 98 % от теоретического. Побочно образуется 0,3–0,4 % о-аминофенола, который можно выделить из кубового остатка, остающегося после перегонки анилина.
По мере потери активности катализатора температура газов на входе в контактный аппарат должна повышаться до 280 °С, причем производительность установки снижается. Катализатор регенерируют 4–5 раз за время работы (регенерацию проводят в токе воздуха с последующим восстановлением оксида меди водородом). Возможна также пропитка катализатора медно-аммиачным раствором. После прохождения через реакторы 4000 т нитробензола катализатор подлежит замене. Расход меди — 1 кг на 1000 кг анилина.
При описанном методе восстановления нитробензола для регулирования температуры в контактном аппарате применяется большой избыток водорода, возвращаемого в процесс после отделения продуктов реакции. При этом во много раз увеличивается объем контактных газов, выходящих из аппарата, и уменьшается концентрация в них анилина. Большой объем газов вызывает необходимость использования громоздких аппаратов на всех стадиях процесса и больших поверхностей теплообмена.
В настоящее время в производстве анилина в качестве реактора используют также кожухотрубчатые контактные аппараты, в трубки которых загружают катализатор. В этом случае регулирование температуры и отвод тепла обеспечиваются высококипящим органическим теплоносителем, которым заполняют межтрубное пространство. Тепло, выделяющееся в процессе восстановления нитробензола, вызывает кипение ВОТ, пары которого поступают в межтрубное пространство парового котла-утилизатора, где теплоноситель конденсируется и стекает обратно в контактный аппарат. Высокий коэффициент теплопередачи от кипящего ВОТ к газам позволяет поднять температуру газов на входе в контактный аппарат значительно выше 170 °С, что, наряду с уменьшением объема газов, повышает производительность контактного аппарата. Такой метод отвода теплоты реакции приводит к снижению капитальных и эксплуатационных расходов.
Парофазное каталитическое восстановление нитробензола является основным методом получения анилина во всем мире. При сравнении технико-экономических показателей производства анилина этим методом и непрерывным методом восстановления нитробензола чугунными стружками в среде электролита было установлено, что метод парофазного каталитического восстановления более экономичен: затраты на 1 т готовой продукции уменьшаются примерно на 15 %, уменьшается также расход энергии. Основной статьей расходов в обоих методах являются расходы на сырье; для улучшения технико-экономических показателей необходимо в первую очередь снижение этих затрат. Использование более селективных катализаторов, уменьшение потерь на каждой стадии процесса, уменьшение осмоления анилина приводят к повышению выхода анилина.
С высоким выходом (97–99 % от теоретического) получается анилин при использовании в качестве катализатора никеля, комбинированного с оксидами ванадия и алюминия. Катализатор работает в относительно широком интервале температур (240–300 °С) и легко регенерируется при окислении воздухом. Описано также производство анилина с использованием подвижного слоя катализатора (медь на силикагеле). Метод позволяет легко отводить выделяющееся при реакции тепло посредством контактных аппаратов с межтрубным пространством, заполненным органическим теплоносителем. В других случаях для отвода тепла используется кипящая вода, дающая перегретый пар.
Если в исходном нитробензоле присутствуют каталитические яды, например сернистые соединения, гидрирование можно вести на сульфидах никеля и молибдена при 350–370 °С и давлении 20–30 МПа, что значительно усложняет аппаратуру.
Восстановление в жидкой фазе.
Каталитическое восстановление нитробензола водородом в жидкой фазе имеет не меньшее значение, чем парофазное восстановление. Этот процесс проходит при более низкой температуре, чем газофазный. Так как один из ингредиентов реакции (водород) газообразен, то для увеличения его концентрации в системе процесс ведут под давлением в автоклавах. В условиях периодического жидкофазного процесса нитросоединение, смешанное с твердым катализатором, обрабатывают водородом под давлением до прекращения поглощения последнего. После отстаивания образовавшегося амина его сифонируют и очищают от катализатора. Через несколько циклов катализатор отфильтровывают и регенерируют. Гидрирование проводят при энергичном перемешивании реакционной массы для равномерного распределения катализатора по всему объему.
Как правило, жидкофазное гидрирование нитросоединений проводят в присутствии растворителя, которым может служить и образующийся в результате реакции амин. Свойства растворителя существенно влияют на скорость гидрирования. Гидрирование быстрее протекает в спиртах и в воде и медленнее — в ароматических углеводородах вследствие их сорбции на активных центрах катализатора. Испытано гидрирование нитросоединений также в водной эмульсии.
Катализаторами жидкофазного гидрирования являются металлический никель (в технике), платина и палладий (в лабораторной практике). Никелевые катализаторы получают восстановлением водородом оксидов никеля, образующихся при прокаливании нитрата, карбоната или оксалата никеля. Активный и стойкий никелевый катализатор может быть получен нагреванием формиата никеля в смеси парафина и парафинового масла до 250 °С с последующей промывкой спиртом и петролейным эфиром. В производственных условиях удобно работать с катализаторами в виде гранул достаточно крупных, чтобы их не уносили потоки жидкости или газа. В этом случае исключается необходимость фильтрования продуктов восстановления и легче организуется непрерывный процесс.
Широкое применение как катализатор гидрирования получил скелетный никелевый катализатор, так называемый никель Ренея. Его получают, обрабатывая никелевоалюминиевый сплав едкой щелочью при нагревании до полного выщелачивания алюминия. Остающийся при этом мелко раздробленный никель обладает очень большой поверхностью и весьма активен. Катализатор сохраняют под водой или под спиртом — сухой катализатор пирофорен. В катализаторе содержится значительное количество водорода, поэтому многие органические соединения можно гидрировать таким катализатором без введения водорода извне. Применение скелетного никелевого катализатора позволяет получать из нитросоединений амины при атмосферном давлении и комнатной температуре. На рис. 4.2.4 представлена одна из промышленных схем восстановления нитробензола в жидкой фазе в присутствии растворителя.
Нитробензол, растворитель (метанол) и катализатор (никель Ренея) смешивают в аппарате 1 и подают в систему реакторов 2–5, одновременно в реакторы подается водород. Реакторы 2–4 имеют высоту около 6 м, в каждом аппарате есть три ряда охлаждающих трубок, в которых циркулирует вода. В реакторе 5, меньшем по размеру, происходит окончательное восстановление нитробензола. Давление в системе 15–20 МПа. Благодаря движению водорода катализатор находится в суспендированном состоянии, а реакционная смесь транспортируется через реакторы. Из сепаратора 8 часть катализаторной суспензии в метанольном растворе анилина насосом 9 направляют на рециркуляцию через смеситель 1. Основное количество реакционной смеси после отстаивания направляют в ректификационную колонну 10, где отгоняют метанол (дефлегматоры и кипятильники колонн на рисунке не показаны). После отгонки метанола в сепараторе 11 расслаивают кубовую жидкость на водный и анилиновый слои. Водный слой поступает в колонну 12, где сверху выводится азеотропная смесь анилина с водой, а из куба выходит вода, направляемая на биохимическую очистку перед спуском в водоем. В колонне 13 отгоняют воду из органического слоя. Водная фракция направляется обратно в сепаратор 11, а органический слой — в колонну 14, где в виде дистиллята отгоняют товарный анилин, а кубовые остатки направляют на сжигание. Выход анилина составляет 99 %.
Жидкофазное гидрирование нитробензола используется и в лабораторной практике, реакцию проводят при относительно невысоких температурах (начиная с комнатной), что благоприятно сказывается на выходе и качестве целевого продукта. Наиболее употребительные катализаторы для жидкофазного гидрирования в лаборатории: никель Ренея и палладий на угле. При проведении гидрирования через жидкую реакционную массу (раствор нитробензола в спирте или его эмульсия в воде), находящуюся в контакте с твердым катализатором, барботируют водород. Для увеличения скорости процесса его практически всегда ведут под давлением водорода. Чтобы обеспечить наилучший контакт водорода, раствора нитросоединения и твердого катализатора, что является важнейшим условием успешного проведения гидрирования, необходимо энергичное перемешивание реакционной массы. Для этого прибегают к специальным размешивающим устройствам или усиленному барботажу водорода, который берут со значительным избытком, а затем рециркулируют.
Аммонолиз фенола
При действии на фенол (8) аммиаком гидроксигруппа замещается на аминогруппу (уравнение (4.2.9)). Эта реакция требует достаточно жестких условий: при пропускании паров фенола и аммиака над катализатором при 425 °С выход анилина составляет 88 %.
Реакция аминирования фенола слабо экзотермична: –Δ = +10 кДж/моль; энергия активации реакции ~117 кДж/моль. Аминирование фенола сопровождается побочными реакциями (уравнения (4.2.10), (4.2.11)) образования дифениламина (9), которые эндотермичны. При температуре более 450 °С происходит диссоциация аммиака на азот и водород (уравнение (4.2.12)).
Несмотря на то, что реакция аминирования фенола известна давно, в промышленности этот способ долгое время не был реализован в основном из-за проблем, связанных с созданием экономичного катализатора, защитой аппаратуры от коррозии и повышением качества готового продукта.
Аминирование фенола чаще всего проводят на кислотных катализаторах; обычно это оксиды алюминия, кремния, титана или циркония, алюмосиликаты, а также фосфорная кислота. Особенно активна система: оксид алюминия (10–20 %) + оксид кремния (90–80 %) — в форме природных или синтетических цеолитов. Чтобы облегчить регенерацию, в катализаторы вводят церий, ванадий, вольфрам или их оксиды, катализирующие процессы окисления. Работают катализаторы при 300–600 °С. Оптимальными условиями считаются 400–480 °С и давление 0,7 МПа и выше. Для предотвращения образования дифениламина при аминировании фенола нужен избыток аммиака, который составляет от 1 до 20 моль на 1 моль фенола. Выход анилина от 88 до 95 %.
Аммонолиз фенола в жидкой фазе проводят в присутствии хлорида, сульфата и нитрата аммония, хлоридов алюминия, железа, меди, ртути, свинца и лития, а также оксида, сульфата и хлорида олова. Процесс ведут в автоклаве при 300–350 °С. Наиболее активен хлорид олова, в присутствии которого получают анилин с выходом 55–56 %.
В первой промышленной установке получения анилина из фенола, пущенной в Японии в 1970 г. фирмой «Halcon International» (США) по технологии, разработанной фирмой «Scientific Design» (США), в качестве катализатора использовался оксид алюминия, полученный из соответствующего геля с содержанием не более 1 % щелочного металла, а также алюмосиликат, содержащий 35–55 % оксида алюминия. Катализатор проработал без замены до 1976 г.
Серьезные затруднения при разработке технологии аминирования фенола были связаны с разделением фенола и анилина, которые образуют азеотропную смесь, содержащую 42 % фенола и кипящую при 186 °С при атмосферном давлении. Это означает, что весь не вступивший в реакцию фенол должен рециркулировать через реактор в виде азеотропной смеси. Поскольку такая смесь содержит большое количество анилина, неизбежно образование дифениламина и потери анилина. Эта проблема в основном была решена за счет высокой степени конверсии фенола.
Смеси, содержащие фенол, являются очень коррозионными при высоких температурах. Поэтому аминирование фенола проводят при относительно низких температурах. Кроме того, при низких температурах продлевается время работы катализатора и уменьшается диссоциация аммиака. Смеси фенола и анилина разделяют при пониженном давлении в колоннах из нержавеющей стали.
Промышленный процесс получения анилина из фенола состоит из следующих основных стадий: 1) аминирование фенола в газовой фазе в присутствии катализатора; 2) отделение избытка аммиака от продуктов реакции и возврат аммиака в реактор; 3) отделение воды от продуктов реакции; 4) разделение анилина и фенола и возврат фенола в реактор. Схема аммонолиза фенола приведена на рис. 4.2.5.
Фенол и жидкий аммиак испаряют частично за счет утилизации теплоты реакции, а частично за счет тепла, подводимого в смеситель 1, и подают в адиабатический трубчатый реактор 2 с неподвижным слоем катализатора. В этот же реактор подают смесь фенола и анилина со стадии выделения азеотропной смеси. Проходя через слой катализатора, фенол, реагируя с аммиаком, превращается в анилин. Процесс проводят при 300–400 °С и давлении 1 МПа. Соотношение фенола и аммиака от 1 : 5 до 1 : 20. Степень превращения фенола 98–99 %.
Продукты реакции частично конденсируются в теплообменнике 3. Жидкую фазу, состоящую в основном из анилина и растворенного аммиака, отделяют и подают в систему ректификационных колонн. В колонне 4 отгоняют аммиак, который возвращается в реактор 2 компрессором 10, некоторое количество аммиака при этом диссоциирует на водород и азот. По мере накопления примесей циркулирующий аммиак сбрасывают в систему очистки отходящих газов. Кубовая жидкость колонны 4 поступает в осушительную колонну 7, в которой отгоняют реакционную воду, а затем в колонну 8. Из колонны 8 анилин отгоняют в виде дистиллята, а с нижних тарелок колонны отбирают азеотропную смесь фенола и анилина, которую возвращают в реактор 2. Из куба колонны 8 выводят остатки, содержащие дифениламин, и направляют их на сжигание. Разделение фенола и анилина для увеличения их относительной летучести проводят в вакууме. Полученный анилин не нуждается в дополнительной очистке.
Расход фенола и аммиака на 1 т. анилина составляет соответственно 1,035 и 0,185 т., что соответствует выходу 97,6 % от теоретического.
Получение анилина из толуола
В начале 1970-х гг. фирма «American Cyanamid» (США) разработала оригинальную технологию получения анилина аммонолизом бензойной кислоты(11). В промышленности бензойную кислоту получают путем жидкофазного окисления толуола (10) в присутствии солей кобальта (уравнение (4.2.13)).
2С6Н5СН3 + 3O2 → 2С6Н5СООН + Н2О | (4.2.13) |
| (10) (11) | |
При действии на бензойную кислоту водным раствором аммиака в присутствии оксида меди(II) при 215–220 °С и 3,5–4,2 МПа образуется анилин. Выход анилина составляет 37 %.
Процесс аммонолиза бензойной кислоты состоит из двух стадий:
1) взаимодействие оксида меди(II), бензойной кислоты и аммиака с образованием анилина (уравнение (4.2.14));
2) регенерация оксида меди(II), т. е. окисление оксида меди(I) кислородом воздуха (уравнение (4.2.15)).
Превращение бензойной кислоты в анилин проходит через стадию образования промежуточного соединения — амида бензойной кислоты (C6H5CONH2; бензамид). В результате внутримолекулярной перегруппировки (реакция Гофмана) образуется анилин и оксид углерода, который окисляется в диоксид.
С6Н5СООН + NH3 + 2CuO → С6Н5NH2 + Cu2O + СO2 + Н2О | (4.2.14) |
| 2Cu2O + O2 → 4CuO | (4.2.15) |
На производстве при получении анилина из толуола (рис. 4.2.6) процесс начинается с приготовления суспензии катализатора в толуоле в аппарате 1, снабженном мешалкой. Катализатором обычно служит нафтенат кобальта. Суспензию направляют в реактор 2, в нижнюю часть которого подают воздух. Окисление толуола проводят при 130–140 °С и 0,21–0,22 МПа. Так как реакция окисления сопровождается большим экзотермическим эффектом, необходимо постоянно отводить тепло. Степень конверсии толуола в бензойную кислоту 30–40 %.
Выходящие из реактора 2 газы направляются в конденсатор 3, в котором конденсируются органические продукты, унесенные отработанным воздухом. Из конденсатора конденсат направляется в жидкостный сепаратор 4 для расслоения на водный и органический слои. Органическую фазу, богатую толуолом, возвращают в реактор, а водную направляют на биохимическую очистку. Газы, выходящие из конденсатора 3, очищаются в угольных адсорберах (на схеме не показаны), где улавливается большая часть органических примесей. Для десорбции уловленных продуктов через адсорберы продувают водяной пар. Полученную смесь расслаивают. Органический слой, содержащий толуол, возвращают в реактор, а воду направляют на биохимическую очистку.
Реакционная масса из реактора 2 после отделения катализатора (методом фильтрования) поступает в отгонную колонну 5, работающую при атмосферном давлении. Дистиллятом является толуол, возвращаемый в реактор. Кубовая жидкость поступает в вакуум-отгонную колонну 6, в которой бензойная кислота отделяется от высококипящих примесей. Бензойная кислота в расплавленном состоянии направляется на стадию аммонолиза для получения анилина.
В абсорбере 7 готовят водный раствор аммиака. Бензойную кислоту, суспензию оксида меди(II) и аммиачную воду подают в реактор 8, снабженный мешалкой и обратным холодильником. Мольное соотношение бензойной кислоты, воды, аммиака и оксида меди составляет 1,5 : 1,8 : 3,4 : 1. Хотя вода и не участвует в реакции, показано, что ее избыток тормозит образование промежуточного соединения — бензамида.
Реакцию аммонолиза проводят при 220 °С и 3,5 МПа, при этом в реакцию вступает 35 % всей поступающей бензойной кислоты, из которой 88 % превращается в анилин. Кроме того, образуется около 10 % фенола и 2 % дифениламина. После аммонолиза реакционную массу отфильтровывают от катализатора и направляют в каскад ректификационных колонн.
Осадок с фильтра 10 поступает в реактор 11 для окисления образовавшегося Cu2O в CuO. Реакция протекает в среде аммиака. В нижнюю часть реактора подают воздух, и там при обычной температуре и атмосферном давлении протекает эндотермическая реакция с полным превращением Cu2O в CuO. Суспензия CuO из реактора 11 возвращается в реактор 8.
Из фильтрата в колонне 12 десорбируют аммиак, который улавливают в абсорбере 7 и возвращают в реакцию. В колонне 13 удаляют воду и возвращают ее на стадию абсорбции аммиака. Небольшая часть воды используется для промывки CuO на фильтрах. В колонне 14 при пониженном давлении отгоняют анилин. Из куба колонны (аппарат 15) при более глубоком вакууме выделяют некоторое количество фенола, анилина, а также бензойную кислоту, возвращаемую в реактор 8, и дифениламин. Кубовые остатки направляют на сжигание.
Суммарный выход анилина в расчете на толуол составляет 79,2 %.
Получение анилина из хлорбензола
Вследствие малой подвижности галогена, связанного с ароматическим ядром, реакция протекает гладко при температуре около 200 °С и давлении 6–10 МПа лишь в присутствии соединений меди. Особенно эффективным катализатором являются соли меди(I).
Скорость реакции прямо пропорциональна концентрации хлорбензола и катализатора и не зависит от концентрации аммиака.
Промышленный процесс проводят в трубчатом аппарате из хромоникелевой стали. Степень коррозии аппаратуры зависит от скорости движения реакционной массы и резко возрастает при Re ≥ 150 000. Реакция хорошо идет уже при скорости, которая обеспечивает устойчивый турбулентный режим (Re ≈ 10 000). При расходе на 1 моль хлорбензола 5 моль аммиака, который берется в виде 34%-ного раствора, и 0,2 моль оксида меди(I) реакция заканчивается через 2–3 ч при 200–230 °С и 7 МПа. В результате образуется около 90 % анилина, 4–5 % фенола и 1–2 % дифениламина. Анилин, полученный из хлорбензола, легко выделяется из реакционной массы путем перегонки и отличается большой стойкостью при хранении.
Этот метод синтеза анилина не получил широкого распространения в промышленности. Лишь одна фирма — «Dow Chemical» (США) — в течение ряда лет получала анилин таким способом, что в основном объясняется наличием у фирмы дешевого хлора. Этот способ получения анилина известен как способ Доу (Dow process). В 1966 г. промышленное производство анилина из хлорбензола фирмой было закрыто.
Замещение сульфогруппы аминогруппой
Сульфогруппу в бензолсульфокислоте(12) можно заменить аминогруппой (уравнение (4.2.17)). В качестве реагента необходимо взять амид щелочного металла, т. к. с аммиаком эта реакция не идет. В условиях сплавления бензолсульфокислоты и амида натрия получается анилин, но выход продукта небольшой.
C6H5SO3Na + NH2Na → С6Н5NH2 + Na2SO3 (4.2.17)
(12)
Значительно с большим выходом идет реакция, если она проводится между солью сульфокислоты и пиперидином натрия в избытке пиперидина, но в промышленности этот метод синтеза анилина практического применения не получил.
C текущей ситуацией и прогнозом развития российского рынка антидетонационных добавок можно познакомиться в отчете Академии Конъюнктуры Промышленных Рынков