ПОЛУЧЕНИЕ И ПРИМЕНЕНИЕ СТИРОЛА
Стирол C6H5CH=CH2 - один из важнейших продуктов нефтехимии, сырье для получения полимеров (полистирол, синтетический каучук) и сополимеров (ударопрочный полистирол на основе акрилонитрила и бутадиена).

Свойства продукта и технические характеристики
Стирол представляет собой прозрачную жидкость. Химическое название и формула: фенилэтилен - C8Н8. Стирол является сырьем для производства самых разнообразных материалов: полистирольных пластмасс, бутадиенстирольных каучуков, лакокрасочных материалов, клеев, АБС-пластиков, термоэластопластов, является растворителем полиэфиров и полиэфирных смол. Отечественная промышленность выпускает стирол двух основных марок: СДЭБ, СДМФК. Стирол легко полимеризуется даже при хранении на холоде. В темноте и при отсутствии катализаторов он постепенно превращается в твердую, прозрачную и бесцветную массу. Стирол хорошо растворяется в ароматических углеводородах и ограниченно в этиленгликоле, пропиленгликоле, диэтиленгликоле, глицерине, пентаэритрите.
Продукт заливают в цистерны или бочки, перевозят железнодорожным или автомобильным транспортом в крытых транспортных средствах, хранят в емкостях из нержавеющей стали или алюминия, в биметаллических емкостях с внутренним алюминиевым покрытием или из углеродистой стали с внутренним специальным покрытием под азотной подушкой. Хранят при температуре не выше 200˚С.
Стирол токсичен. При вдыхании паров наблюдаются головные боли, при длительном воздействии - заболевания печени и нервной системы. При работе со стиролом следует защищать кожу рук резиновыми перчатками, а в случае больших концентраций пользоваться противогазом.
Приведены физико-химические показатели стирола как товарного продукта по ГОСТ 10003-90.
Техническая характеристика стирола (согласно ГОСТ 10003-90)
Показатель | Значение | Метод испытаний | |
| СДЭБ | СДМФК | ||
| Внешний вид | Прозрачная однородная жидкость без нерастворенной влаги и механических примесей | п. 3.2 ГОСТ | |
| Массовая доля стирола, %, не менее | 99,80 | 99,80 | п. 3.3 ГОСТ |
| Массовая доля фенилацетилена, %, не более | 0,01 | - | п. 3.3 ГОСТ |
| Массовая доля метилэтилакролеина, %, не более | - | 0,006 | п. 3.3 ГОСТ |
| Массовая доля дивинилбензола, %, не более | 0,0005 | - | п. 3.3 ГОСТ |
| Массовая доля ацетофенона, %, не более | - | 0,006 | п. 3.3 ГОСТ |
| Массовая доля карбонильных соединений в пересчете на бензальдегид, %, не более | 0,01 | 0,01 | п. 3.4 ГОСТ |
| Массовая доля перекисных соединений в пересчете на активный кислород, %, не более | 0,0005 | 0,0005 | п. 3.5 ГОСТ |
| Массовая доля полимера, %, не более | 0,001 | 0,001 | п. 3.6 ГОСТ |
| Цветность по платиново-кобальтовой шкале, ед. Хазена, не более | 10 | 10 | п. 3.7 ГОСТ |
| Массовая доля стабилизатора пара-трет-бутилпирокатехина, % | 0,0005 - 0,0010 | 0,0005 - 0,0010 | п. 3.8 ГОСТ |
Области применения стирола
Стирол применяют для производства различных полимеров: от эластичной пены до высококачественных технических пластмасс. В основном стирол расходуется на производство полистирола, обладающего высокой химической и водостойкостью, низкой стоимостью, является диэлектриком. Конечные варианты применения стирола: одноразовая посуда, упаковка для электронного оборудования, компоненты автомобильных салонов.
Технологии производства стирола
Основным промышленным способом производства стирола является в настоящее время дегидрирование этилбензола. Перспективным может быть получение стирола из фракции C8 пиролизной смолы.
Дегидрирование этилбензола в стирол протекает по реакции: C6H5CH2CH2 ⇄ C6H5CH=CH2 + H2.
Реакция - эндотермическая и протекает с увеличением объема. Соответственно с повышением температуры и снижением парциального давления углеводорода увеличивается степень превращения этилбензола в стирол. При давлении 0,1 МПа эта зависимость выглядит так:
Температура дегидрирования, К 700 800 900 1000
Равновесная степень превращения 0,055 0,21 0,53 0,83
Для увеличения глубины превращения сырье разбавляют водяным паром, что эквивалентно снижению давления реагирующей смеси. Так, при 900К равновесная степень дегидрирования этилбензола в стирол в зависимости от разбавления водяным паром возрастает следующим образом:
Мольное соотношение H2O : C6H5CH=CH2 0 5 10 20
Равновесная степень дегидрирования 0,53 0,77 0,85 0,9
C6H5C2H5 → C6H5CH=CH2 + H2 (стирол)
C6H5C2H5 → C6H6 + C2H4 (бензол)
C6H5C2H5 → C6H5CH3 + СH4 (толуол)
C6H5C2H5 → C6H6 + C2H6 (бензол)
C6H5C2H5 → 7C + CH4 + 3H2
В промышленности используют разбавление водяным паром в соотношении пар : газ = (15-20) : 1 и реакцию проводят при температуре 830-900 К. Катализаторы приготавливают на основе оксида железа с добавками K и Cr.
Избирательность по стиролу составляет около 98%. Кроме реакции распада на катализаторе образуются углистые отложения. Водяной пар, подаваемый на разбавление, не только сдвигает равновесие, но и газифицирует углистые отложения на поверхности катализатора. Протекает непрерывная регенерация катализатора, и срок его службы составляет 1,5-2 года.
На Рис.1 приведена технологическая схема дегидрирования этилбензола
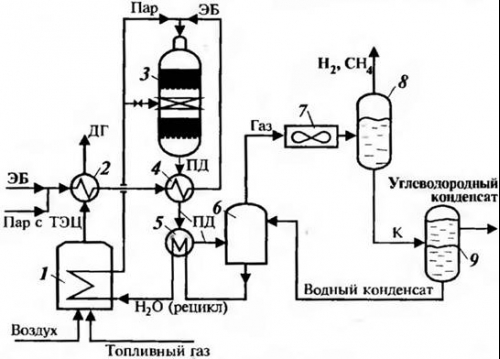
Рис. 1. Схема дегидрирования этилбензола в стирол:
1 - пароперегревательная печь; 2 - испаритель этилбензола; 3 - реактор дегидрирования; 4 - подогреватель этилбензола; 5 - подогреватель воды; б - пенный аппарат; 7 - воздушный холодильник; 8- сепаратор; 9 - разделитель фаз. Потоки: ЭБ - этилбензол (свежий и рецикл); Н2, СН4 - горючие газы в топливную сеть; ДГ - дымовые газы; К - конденсат; ПД - продукты дегидрирования.
Эффективность тепловой схемы агрегата дегидрирования этилбензола может быть оценена с помощью теплового КПД.
В промышленных агрегатах дегидрирования этилбензола тепловой КПД, как правило, не превышает 28-33%. Анализ показывает, что главная причина низкой тепловой эффективности связана с отсутствием рекуперации тепла низкотемпературного контактного газа.
Значительно улучшить использование энергетического потенциала процесса можно в энерготехнологической системе. Пример такой системы в производстве стирола интересен тем, что он вытекает из физико-химического анализа условий реакции дегидрирования. Как отмечено выше, разбавление этилбензола водяным паром преследует две цели: сдвинуть равновесие реакции вправо и создать условия непрерывной регенерации катализатора. Сам же водяной пар в реакции не участвует; его приходится получать испарением воды и потом отделять от продуктов реакции конденсацией. Несмотря на регенерацию тепла потоков, испарение и нагрев, охлаждение и конденсация - процессы в производстве термодинамически необратимые, и энергетический потенциал используется далеко не полностью.
Такое же влияние на процесс, как и водяной пар, может оказать и другой компонент, например CO2. Он инертен в реакции, т. е. может быть разбавителем, и способствует регенерации катализатора, взаимодействуя с углистыми отложениями. Получают СO2 сжиганием топливного газа. Продукты горения являются энергоносителем. Это дополнительное свойство разбавителя позволяет создать энерготехнологическую схему производства стирола.
В энерготехнологической схеме есть еще ряд узлов - для нагрева этилбензола, воздуха, топливного газа, использующих тепло нагретых потоков. Последние необходимы, чтобы сбалансировать тепловые потоки всей ХТС. Данный метод получения стирола дегидрированием этилбензола позволяет увеличить энергетический КПД почти вдвое - до 70%.
C текущей ситуацией и прогнозом развития российского рынка стирола можно познакомиться в отчете Академии Конъюнктуры Промышленных Рынков «Рынок стирола в России».